Die neuen im New England Journal of Medicine veröffentlichten Daten zeigen: Patienten mit
metastasiertem kastrationsresistentem Prostatakarzinom, die mit Docetaxel vorbehandelt
waren und innerhalb von 12 Monaten unter einem auf den Androgenrezeptor (AR) gerichteten
Wirkstoff (Abirateron oder Enzalutamid) eine Progression erlitten, haben bei Behandlung
mit Jevtana® (Cabazitaxel) in Kombination mit Prednison ein signifikant längeres radiologisch
progressionsfreies Überleben (rPFS). Als Vergleich diente hier Abirateron in Kombination mit
Prednison oder Enzalutamid. Das Gesamtüberleben (OS) war mit Cabazitaxel ebenfalls signifikant
verlängert. Diese Ergebnisse aus der CARD-Studie wurden nun im Rahmen des Presidental
Symposiums auf der Jahrestagung der European Society of Medical Oncology (ESMO) 2019
in Barcelona, Spanien, vorgestellt.
CARD ist eine randomisierte, unverblindete klinische Behandlungssequenzstudie unter Beteiligung
von 62 Prüfzentren in 13 europäischen Ländern, in die 255 Patienten (medianes Alter 70 Jahre,
31 Prozent über 75 Jahre) mit mCRPC aufgenommen wurden, welche vorab mit Docetaxel behandelt
waren und die innerhalb von 12 Monaten unter einem AR-gerichteten Wirkstoff eine Progression
erlitten, unabhängig von der Reihenfolge der Behandlungen. Diese Patienten wurden 1:1 auf
Cabazitaxel (25 mg/m2 intravenös alle drei Wochen, Prednison täglich und
Granulozyten-Kolonie-stimulierender Faktor) oder zum Vergleich auf Abirateron
(1.000 mg plus Prednison, täglich) bzw. Enzalutamid (160 mg täglich) randomisiert
(Abirateron bei Vorbehandlung mit Enzalutamid bzw. Enzalutamid bei Vorbehandlung
mit Abirateron).
Der primäre Endpunkt der Studie war das rPFS, das unter Behandlung mit Cabazitaxel (n=129)
im Vergleich zu Abirateron oder Enzalutamid um das mehr als Zweifache länger ausfiel
(n=126; Median 8,0 vs. 3,7 Monate; HR=0,54; 95 Prozent-KI: 0,400,73; p<0,0001).
Mit Cabazitaxel behandelte Patienten erlebten eine Verbesserung des rPFS in allen
vorab festgelegten Subgruppen, unabhängig vom Zeitpunkt des vorherigen alternativen
AR-gerichteten Wirkstoffs vor oder nach Docetaxel. Cabazitaxel verbesserte zudem
signifikant einen wichtigen sekundären Endpunkt, das OS (Median 13,6 vs. 11,0 Monate;
HR=0,64; 95 Prozent-KI: 0,460,89; p=0,0078) und reduzierte das Gesamtmortalitätsrisiko
im Vergleich zu Abirateron oder Enzalutamid um 36 Prozent. Weitere wichtige sekundäre
Endpunkte fielen ausnahmslos zugunsten von Cabazitaxel aus: Das progressionsfreie
Überleben (PFS) (Median 4,4 vs. 2,7 Monate; p<0,0001), das bestätigte PSA-Ansprechen
(35,7 vs. 13,5 Prozent; p=0,0002) und das Tumoransprechen
(36,5 vs. 11,5 Prozent; p=0,004). Auch das Schmerzansprechen (45,0 vs. 19,3 Prozent; p<0,0001)
und die Zeit bis zu symptomatischen skelettalen Ereignissen (nicht erreicht vs. 16,7 Monate, p=0,0499)
verbesserten sich unter Behandlung mit Cabazitaxel signifikant.
Die Inzidenz unerwünschter Ereignisse von Grad ≥3 betrug 56,3 Prozent unter
Cabazitaxel vs. 52,4 Prozent unter AR-gerichteten Wirkstoffen. Die für Cabazitaxel
wichtigsten unerwünschten Arzneimittelwirkungen von Grad ≥3 im Vergleich zu AR-gerichteten
Wirkstoffen umfassten Erkrankungen der Niere (3,2 Prozent vs. 8,1 Prozent),
Infektionen (7,9 Prozent vs. 7,3 Prozent), Muskel-/Skelett-Schmerzen/Beschwerden
(1,6 Prozent vs.
Sanofi-Aventis Deutschland GmbH / SADE.CAB.19.09.2523 (10/19)
Quelle:
29. Oktober 2019
CARD-Studie erreicht primären Endpunkt und weitere sekundäre Endpunkte
Abb.: Das mediane progressionsfreie Überleben (rPFS) betrug unter Behandlung mit
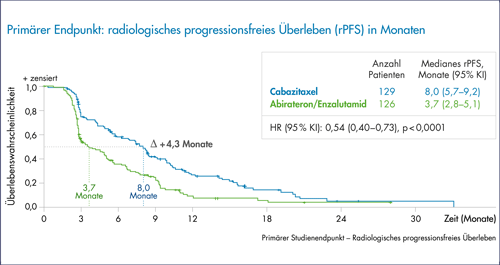
Cabazitaxel 8,0 Monate vs. 3,7 Monate unter Abirateron oder Enzalutamid.
5,6 Prozent), Herzerkrankungen (0,8 Prozent vs. 4,8 Prozent),
asthenische Störungen
(4,0 Prozent vs. 2,4 Prozent), Diarrhö (3,2 Prozent vs. 0 Prozent),
periphere Neuropathie (3,2 Prozent vs. 0 Prozent) und febrile Neutropenie
(3,2 Prozent vs. 0 Prozent). Die Raten schwerwiegender unerwünschter Ereignisse
jeden Grads waren für die Behandlung mit Cabazitaxel (38,9 Prozent) ähnlich wie
bei Behandlung mit AR-gerichteten Wirkstoffen
(38,7 Prozent). Unerwünschte
Ereignisse führten bei Cabazitaxel zum Tod von 7 Patienten, verglichen mit
14 Patienten bei AR-gerichteten Wirkstoffen (5,6 Prozent vs. 11,3 Prozent).
Es wurden keine neuen Sicherheitssignale beobachtet.
de Wit R, de Bono J, Sternberg CN, Fizazi K, Tombal B, et al. 2019.
Cabazitaxel versus Abiraterone or Enzalutamide in Metastatic Prostate Cancer. NEJM, DOI: 10.1056/NEJMoa1911206
Mit Cabazitaxel stieg das radiologisch progressionsfreie Überleben (primärer Endpunkt)
um mehr als das Doppelte und das Mortalitätsrisiko (wichtiger sekundärer Endpunkt)
reduzierte sich signifikant um
36 Prozent
Die Studienergebnisse wurden im Rahmen des Presidental Symposiums auf der Jahrestagung
der European Society of Medical Oncology 2019 vorgestellt
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz