
Metastasiertes Nierenzellkarzinom
Real-World-Daten zur IO-basierten Therapie
Immunbasierte (IO)-Kombinationen bilden das Rückgrat in der systemischen Therapie des metastasierten Nierenzellkarzinoms (mNZK). Neben den Daten aus klinischen Phase-III-Studien sind auch die klinische Praxis widerspiegelnde Real-World-Daten von speziellem Interesse.
In die retrospektive Studie gingen Daten von 201 mNZK-Patienten ein, die ab Januar 2006 eine systemische Erstlinientherapie erhalten hatten. Es wurden klinisch-pathologische und behandlungsbezogene Daten erfasst. Das progressionsfreie Überleben (PFS) und das Gesamtüberleben (OS) wurden mittels deskriptiver Statistik und Kaplan-Meier-Schätzung analysiert.
Patientencharakteristika
Im Gesamtkollektiv hatten 76 Patienten in der Erstlinie eine IO-basierte Therapie (55 eine IO-IO, 21 eine TKI-IO-Kombination) und 125 eine TKI-Monotherapie (TKI-Mono).
Von der initialen Diagnose bis zum Beginn einer systemischen Therapie verstrichen bei einer TKI-Mono median 14,3 Monate und 7,8 Monate bei einer IO-basierten Therapie (IO-IO 4,4 und TKI-IO 26,8 Monate). Die Auflistung der Patienten gemäß MSKCC-Kriterien ergab, dass 13 Patienten (17,1%) mit IO-basierter Therapie der günstigen Risikogruppe zugeordnet worden waren, ebenso 9 Patienten, die mit einer TKI-IO und 4 Patienten, die mit einer IO-IO-Kombination behandelt worden waren. Nur 9 Patienten, die eine TKI-Mono erhalten hatten, waren in die günstige MSKCC-Risikogruppe eingestuft worden. Patienten mit IO-basierter Erstlinientherapie hatten mehrheitlich eine synchrone Erkrankung (54,0 vs. 45,6%) mit mehreren betroffenen Organsystemen (67,1 vs. 49,6%).
Überlebensanalysen
Insgesamt betrug die mediane Zeit einer systemischen Erstlinientherapie 6,4 Monate (7,3 Monate bei einer TKI-Mono und 5,7 Monate bei einer IO-basierten Behandlung; 4,6 Monate mit IO-IO und 12,3 Monate mit TKI-IO). Mit einer Erstlinien-TKI-IO verbesserte sich das PFS gegenüber einer TKI-Mono (23,9 vs. 10,3 Monate, HR 0,48, p=0,034p=0,012). In multivariater Analyse wurde ein signifikant verbessertes PFS für TKI-IO vs. einer IO-IO-Kombination wie auch TKI-IO vs. TKI-Mono bestätigt (HR 0,37, p=0,023 bzw. HR 0,48, p=0,057p=0,099). Das OS war mit der TKI-IO-Kombination länger als mit der TKI-Mono (nicht erreicht vs. 2,64 Jahre, HR 0,37, p=0,050). Allerdings bestand ein numerischer Vorteil der TKI-IO-Kombination gegenüber der IO-IO-Kombination (HR 0,45, p=0,183). Bei Patienten mit günstigem versus intermediärem/schlechtem MSKCC-Risiko betrug das mediane OS 5,04 bzw. 2,63 Jahre (HR 0,38, p=0,020).
Nivolumab-Subgruppe
In einer Subanalyse von Nivolumab nach der Erstlinientherapie (n=40), hatten 21 Patienten Nivolumab in der Zweitlinie und 19 Patienten in einer späteren Linie erhalten (3. Linie n=15, 4. Linie n=1, 5. Linie n=1, 6. Linie n=2). Alle Patienten waren zuvor nur mit einer TKI-Mono oder einem mTOR-Inhibitor behandelt worden. Im ganzen Kollektiv (n=40) wie auch bei Nivolumab in der Zweitlinie (n=21) wurde jeweils ein PFS von 5,5 Monaten registriert. In der dritten Linie erreichte das PFS 4,3 Monate (n=19). Kein signifikanter PFS-Unterschied bestand zwischen Nivolumab und TKI-Mono als Zweitlinie (p=0,91 bzw. p=0,579). Der Zusatz von Nivolumab, ob in der Zweitlinie oder darüber hinaus, führte zu signifikant verbessertem Gesamt-überleben verglichen mit wiederholten TKI- oder mTOR-Therapien alleine (2 TKI; median 6,13 vs. 2,61 Jahre, HR, 0,46, p=0,003).
Stühler V, Herrmann L, Rausch S, et al. 2023. Real world data on IO-based therapy for metastatic renal cell carcinoma. J Cancer Res Clin Oncol 149:32493258.
 März 2024
Red.
März 2024
Red.
Real-World-Daten zur IO-basierten Therapie
Immunbasierte (IO)-Kombinationen bilden das Rückgrat in der systemischen Therapie des metastasierten Nierenzellkarzinoms (mNZK). Neben den Daten aus klinischen Phase-III-Studien sind auch die klinische Praxis widerspiegelnde Real-World-Daten von speziellem Interesse.
In die retrospektive Studie gingen Daten von 201 mNZK-Patienten ein, die ab Januar 2006 eine systemische Erstlinientherapie erhalten hatten. Es wurden klinisch-pathologische und behandlungsbezogene Daten erfasst. Das progressionsfreie Überleben (PFS) und das Gesamtüberleben (OS) wurden mittels deskriptiver Statistik und Kaplan-Meier-Schätzung analysiert.
Patientencharakteristika
Im Gesamtkollektiv hatten 76 Patienten in der Erstlinie eine IO-basierte Therapie (55 eine IO-IO, 21 eine TKI-IO-Kombination) und 125 eine TKI-Monotherapie (TKI-Mono).
Von der initialen Diagnose bis zum Beginn einer systemischen Therapie verstrichen bei einer TKI-Mono median 14,3 Monate und 7,8 Monate bei einer IO-basierten Therapie (IO-IO 4,4 und TKI-IO 26,8 Monate). Die Auflistung der Patienten gemäß MSKCC-Kriterien ergab, dass 13 Patienten (17,1%) mit IO-basierter Therapie der günstigen Risikogruppe zugeordnet worden waren, ebenso 9 Patienten, die mit einer TKI-IO und 4 Patienten, die mit einer IO-IO-Kombination behandelt worden waren. Nur 9 Patienten, die eine TKI-Mono erhalten hatten, waren in die günstige MSKCC-Risikogruppe eingestuft worden. Patienten mit IO-basierter Erstlinientherapie hatten mehrheitlich eine synchrone Erkrankung (54,0 vs. 45,6%) mit mehreren betroffenen Organsystemen (67,1 vs. 49,6%).
Überlebensanalysen
Insgesamt betrug die mediane Zeit einer systemischen Erstlinientherapie 6,4 Monate (7,3 Monate bei einer TKI-Mono und 5,7 Monate bei einer IO-basierten Behandlung; 4,6 Monate mit IO-IO und 12,3 Monate mit TKI-IO). Mit einer Erstlinien-TKI-IO verbesserte sich das PFS gegenüber einer TKI-Mono (23,9 vs. 10,3 Monate, HR 0,48, p=0,034p=0,012). In multivariater Analyse wurde ein signifikant verbessertes PFS für TKI-IO vs. einer IO-IO-Kombination wie auch TKI-IO vs. TKI-Mono bestätigt (HR 0,37, p=0,023 bzw. HR 0,48, p=0,057p=0,099). Das OS war mit der TKI-IO-Kombination länger als mit der TKI-Mono (nicht erreicht vs. 2,64 Jahre, HR 0,37, p=0,050). Allerdings bestand ein numerischer Vorteil der TKI-IO-Kombination gegenüber der IO-IO-Kombination (HR 0,45, p=0,183). Bei Patienten mit günstigem versus intermediärem/schlechtem MSKCC-Risiko betrug das mediane OS 5,04 bzw. 2,63 Jahre (HR 0,38, p=0,020).
|
|
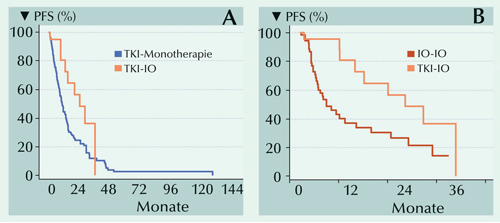
Abb.: Kaplan-Meier-Schätzungen des PFS in Abhängigkeit von der systemischen Erstlinientherapie mit
TKI-IO vs. TKI-Monotherapie (A) und TKI-IO vs. IO-IO-Kombination (B).
|
Nivolumab-Subgruppe
In einer Subanalyse von Nivolumab nach der Erstlinientherapie (n=40), hatten 21 Patienten Nivolumab in der Zweitlinie und 19 Patienten in einer späteren Linie erhalten (3. Linie n=15, 4. Linie n=1, 5. Linie n=1, 6. Linie n=2). Alle Patienten waren zuvor nur mit einer TKI-Mono oder einem mTOR-Inhibitor behandelt worden. Im ganzen Kollektiv (n=40) wie auch bei Nivolumab in der Zweitlinie (n=21) wurde jeweils ein PFS von 5,5 Monaten registriert. In der dritten Linie erreichte das PFS 4,3 Monate (n=19). Kein signifikanter PFS-Unterschied bestand zwischen Nivolumab und TKI-Mono als Zweitlinie (p=0,91 bzw. p=0,579). Der Zusatz von Nivolumab, ob in der Zweitlinie oder darüber hinaus, führte zu signifikant verbessertem Gesamt-überleben verglichen mit wiederholten TKI- oder mTOR-Therapien alleine (2 TKI; median 6,13 vs. 2,61 Jahre, HR, 0,46, p=0,003).
❏ Das Gesamtüberleben in einem Real-World-Umfeld verlängerten sowohl IO-basierte Kombinationen in der Erstlinie als auch Nivolumab nach einer
Erstlinien-TKI-Monotherapie.
❏ Die Analyse lässt einen Vorteil von IO-basierten Kombinationen gegenüber einer TKI-Monotherapie in der Erstlinie erkennen, der bei längerem Follow-up von mNZK-Patienten im Real-World-Umfeld hervortritt.
Stühler V, Herrmann L, Rausch S, et al. 2023. Real world data on IO-based therapy for metastatic renal cell carcinoma. J Cancer Res Clin Oncol 149:32493258.
© 2003-2026 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz