
ESMO 2023
Prostatakarzinom
Radioligandentherapie bei metastasiertem kastrationsresistentem Prostatakarzinom
Die zielgerichtete Radioligandentherapie mit 177Lu-PSMA-617 ist nach Androgenrezeptor (AR)-Inhibition eine Alternative zum Wechsel auf einen anderen AR-Inhibitor. Dies zeigt die Studie PSMAfore mit Erreichen ihres primären sowie wichtigen sekundären Endpunkten.
In der offenen Phase-III-Studie PSMAfore erhielten Taxan-naive Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) 6 Zyklen 177Lu-PSMA-617 (q1w) oder Abirateron bzw. Enzalutamid, entsprechend der vorangegangenen Therapie. Randomisiert wurden 468 Patienten, die laut Einschlusskriterien ≥1 PSMA-positive Läsionen aufwiesen und nach einer vorangegangenen Behandlung mit einem AR-Inhibitor der zweiten Generation progredient waren. Voraussetzung für den Studieneinschluss war außerdem, dass die Patienten Kandidaten für einen AR-Inhibitor-Wechsel, aber keine Kandidaten für eine PARP-Inhibitor-Therapie waren. Eine (neo)adjuvante Chemotherapie >12 Monate vor Studieneinschluss war erlaubt.
Die Patienten waren median 71-72 Jahre alt und hatten in den Studienarmen zu 50,9% bzw. 55,6% eine Behandlung mit Abirateron und zu 40,2% bzw. 35,9% mit Enzalutamid erhalten. Zum Zeitpunkt der zweiten Interimsanalyse, die beim ESMO 2023 präsentiert wurde, wiesen 21,8% der Patienten im 177Lu-PSMA-617-Arm versus 62,4% der Patienten im Kontrollarm einen radiologischen Progress auf. 84,2% der im Kontrollarm progredienten Patienten wechselten zur Therapie mit 177Lu-PSMA-617.
Die Studie erreichte ihren primären Endpunkt mit einer Risikoreduktion für einen radiologischen Progress um 57% (HR=0,43; 95% KI 0,33-0,54; p<0,0001) (Abb.). Im Median zeigten Patienten im 177Lu-PSMA-617-Arm ein radiologisches progressionsfreies Überleben (rPFS) von 12,02 Monaten versus 5,59 Monaten im Kontrollarm. Ein Ansprechen wurde bei 50,7% versus 14,9% der Patienten beobachtet, mit einer medianen Dauer von 13,63 versus 10,05 Monaten. 21,1% versus 2,7% der Patienten erreichten ein komplettes Ansprechen. Eine bestätigte Tumorschrumpfung um ≥50% zeigten 57,6% versus 20,4% der Patienten. Auch die Zeit bis zum ersten symptomatischen skelettalen Ereignis (HR=0,35; 95% KI 0,22-0,57) und bis zur Verschlechterung der Schmerzen (BPI-SF: HR=0,69; 95% KI 0,56-0,85; FACT-P: HR=0,59; 95% KI 0,47-0,72) war unter 177Lu-PSMA-617 gegenüber einem AR-Inhibitor-Wechsel verlängert.
Die zweite Zwischenanalyse bezüglich des OS zeigte für die Cross-over-adjustierte Auswertung einen Trend mit Vorteil für 177Lu-PSMA-617 (HR=0,80; 95% KI 0,48-1,33), aber keinen Unterschied in der Auswertung der ITT-Population (HR=1,16; 95% KI 0,83-1,64). Es wurden im 177Lu-PSMA-617-Arm weniger häufig Nebenwirkungen Grad 3-4 (33,9 vs. 43,1%) und klinisch relevante Nebenwirkungen (20,3 vs. 28,0%) berichtet. Eine Dosisanpassung aufgrund von Nebenwirkungen wurde für 3,5% versus 15,1% der Patienten beschrieben. Es brachen 5,7% versus 5,2% der Patienten die Therapie aufgrund von Nebenwirkungen ab.
 Dez. 2023
IS
Dez. 2023
IS
Prostatakarzinom
Radioligandentherapie bei metastasiertem kastrationsresistentem Prostatakarzinom
Die zielgerichtete Radioligandentherapie mit 177Lu-PSMA-617 ist nach Androgenrezeptor (AR)-Inhibition eine Alternative zum Wechsel auf einen anderen AR-Inhibitor. Dies zeigt die Studie PSMAfore mit Erreichen ihres primären sowie wichtigen sekundären Endpunkten.
In der offenen Phase-III-Studie PSMAfore erhielten Taxan-naive Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom (mCRPC) 6 Zyklen 177Lu-PSMA-617 (q1w) oder Abirateron bzw. Enzalutamid, entsprechend der vorangegangenen Therapie. Randomisiert wurden 468 Patienten, die laut Einschlusskriterien ≥1 PSMA-positive Läsionen aufwiesen und nach einer vorangegangenen Behandlung mit einem AR-Inhibitor der zweiten Generation progredient waren. Voraussetzung für den Studieneinschluss war außerdem, dass die Patienten Kandidaten für einen AR-Inhibitor-Wechsel, aber keine Kandidaten für eine PARP-Inhibitor-Therapie waren. Eine (neo)adjuvante Chemotherapie >12 Monate vor Studieneinschluss war erlaubt.
Die Patienten waren median 71-72 Jahre alt und hatten in den Studienarmen zu 50,9% bzw. 55,6% eine Behandlung mit Abirateron und zu 40,2% bzw. 35,9% mit Enzalutamid erhalten. Zum Zeitpunkt der zweiten Interimsanalyse, die beim ESMO 2023 präsentiert wurde, wiesen 21,8% der Patienten im 177Lu-PSMA-617-Arm versus 62,4% der Patienten im Kontrollarm einen radiologischen Progress auf. 84,2% der im Kontrollarm progredienten Patienten wechselten zur Therapie mit 177Lu-PSMA-617.
|
|
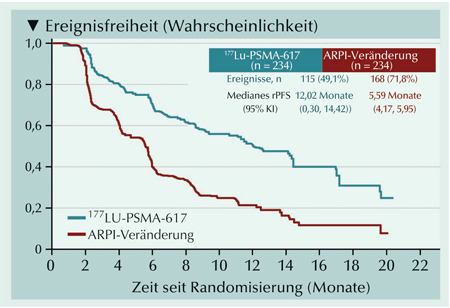
Abb.: Radiologisches progressionsfreies Überleben (rPFS) mit 177Lu-PSMA-617
versus AR-Inhibitor-Wechsel nach AR-Inhibitor-Vortherapie.
|
Die Studie erreichte ihren primären Endpunkt mit einer Risikoreduktion für einen radiologischen Progress um 57% (HR=0,43; 95% KI 0,33-0,54; p<0,0001) (Abb.). Im Median zeigten Patienten im 177Lu-PSMA-617-Arm ein radiologisches progressionsfreies Überleben (rPFS) von 12,02 Monaten versus 5,59 Monaten im Kontrollarm. Ein Ansprechen wurde bei 50,7% versus 14,9% der Patienten beobachtet, mit einer medianen Dauer von 13,63 versus 10,05 Monaten. 21,1% versus 2,7% der Patienten erreichten ein komplettes Ansprechen. Eine bestätigte Tumorschrumpfung um ≥50% zeigten 57,6% versus 20,4% der Patienten. Auch die Zeit bis zum ersten symptomatischen skelettalen Ereignis (HR=0,35; 95% KI 0,22-0,57) und bis zur Verschlechterung der Schmerzen (BPI-SF: HR=0,69; 95% KI 0,56-0,85; FACT-P: HR=0,59; 95% KI 0,47-0,72) war unter 177Lu-PSMA-617 gegenüber einem AR-Inhibitor-Wechsel verlängert.
Die zweite Zwischenanalyse bezüglich des OS zeigte für die Cross-over-adjustierte Auswertung einen Trend mit Vorteil für 177Lu-PSMA-617 (HR=0,80; 95% KI 0,48-1,33), aber keinen Unterschied in der Auswertung der ITT-Population (HR=1,16; 95% KI 0,83-1,64). Es wurden im 177Lu-PSMA-617-Arm weniger häufig Nebenwirkungen Grad 3-4 (33,9 vs. 43,1%) und klinisch relevante Nebenwirkungen (20,3 vs. 28,0%) berichtet. Eine Dosisanpassung aufgrund von Nebenwirkungen wurde für 3,5% versus 15,1% der Patienten beschrieben. Es brachen 5,7% versus 5,2% der Patienten die Therapie aufgrund von Nebenwirkungen ab.
❏ Die PSMAfore-Studie erreichte ihren primären Endpunkt. Nach Progress unter einem AR-Inhibitor wurde bei Taxan-naiven
mCRPC-Patienten ein verlängertes rPFS unter Therapie mit 177Lu-PSMA-617 im Vergleich zum Wechsel auf einen anderen AR-Inhibitor
beobachtet. Das Nebenwirkungsprofil war vorteilhafter unter der Radioligandentherapie.
Sartor O, et al. 2023.
Phase III trial of [177Lu]Lu-PSMA-617 in taxane-naive patients with metastatic castration-resistant prostate cancer (PSMAfore). ESMO 2023, Abstr. #LBA13
© 2003-2026 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz