|
Late-Breaking-News vom EAU 2015 |
|||
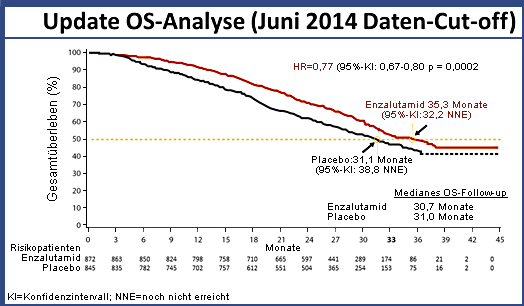
Der Im Rahmen der Late-Breaking-News-Session am letzten Tag der EAU-Jahrestagung in Madrid präsentierte Professor Dr. Bertrand Tombal, Brüssel, Belgien, die jüngsten Ergebnisse der PREVAIL-Studie ein Update der Überlebensanalyse. Die Auswertung nach 784 Todesfällen zeigt einen signifikanten Überlebensvorteil von vier Monaten für Enzalutamid im Vergleich zu Placebo und das obwohl viele Patienten zum Zeitpunkt der Update-Analyse bereits zusätzliche Therapien erhielten [1]. Dies bestätigt Tombal zufolge die Robustheit der Ergebnisse der ersten Auswertung. Basis der von Beer et al. 2014 publizierten Ergebnisse der PREVAIL-Studie war eine Interimsanalyse nach 540 Todesfällen (Daten-Cut-off im September 2013).2 Weil der Vorteil von Enzalutamid gegenüber Placebo bereits damals so deutlich war, wurde die Studie entblindet und die Ergebnisse als endgültig definiert. Patienten aus dem Placebo-Arm konnten in den Enzalutamid-Arm wechseln. Nach 784 Todesfällen wurde jetzt ein Update der Analyse des Gesamtüberlebens (OS) vorgenommen. Daten-Cut-off war im Juni 2014 [1]. Vorteil Enzalutamid: Plus vier Monate beim Gesamtüberleben
Wie in der Interimsanalyse war auch in diesem Update der Überlebensvorteil unabhängig von ECOG-Status,
Alter (über oder unter 75 Jahre), der geographischen Region oder der Tatsache, ob eine viszerale Erkrankung
vorlag oder nicht. 26% der Patienten, die seit Beginn der PREVAIL-Studie Enzalutamid erhalten hatten,
waren im Juni 2014 immer noch unter der Therapie mit dem Androgenrezeptor-Signalweginhibitor [1].
Die positiven Ergebnisse beim OS-Update fügen sich nahtlos die anderen positiven Ergebnisse der PREVAIL-Studie ein [1, 2]: Häufigste Nebenwirkung unter Enzalutamid war Fatigue, die bei etwa einem Drittel der Patienten auftrat
(35,6% vs. 26% unter Placebo) [1, 2]. In die globale Phase-3-Studie PREVAIL wurden 1.717 Männer mit progressivem mCRPC eingeschlossen. Die Patienten waren asymptomatisch oder zeigten einen mild symptomatischen Verlauf und hatten bisher noch keine zytotoxische Chemotherapie erhalten. Sie wurden randomisiert entweder mit 160 mg/d Enzalutamid (n=872) oder Placebo (n=845) behandelt. Co-primäre Endpunkte der Studie waren OS und rPFS [2]. | |||
|
Literatur: [1] Tombal B, et al. 2015. Late Breaking News Plenary Session im Rahmen der Jahrestagung der European Association of Urology (EAU), 24. März 2015, Madrid, Spanien. [2] Beer TM, et al. 2014. N Engl J Med 371:424-433. |
|||
|
|||