Neudefiniertes Kastrationsniveau von unter 20 ng/dl (0,7 nmol/l): Verzögerte Progression, verlängertes Überleben
Das Ziel der chirurgischen Kastration oder der Androgendeprivationstherapie (ADT) ist es,
den Testosteronspiegel von Patienten mit Prostatakarzinom (PCa) unter das Kastrationsniveau zu senken.
Eine neuere Untersuchung zeigt, dass die Einhaltung des laut aktueller EAU-Guideline empfohlenen
Kastrationsniveaus von unter 20ng/dl (0,7nmol/l) im ersten Jahr der Therapie das Überleben der
Patienten und die Sensitivität auf die ADT verlängert.
In der Behandlung des hormonabhängigen Prostatakarzinoms gilt die ADT als das Mittel der
Wahl [1]. Mittels chirurgischer Kastration wird durchschnittlich ein Testosteronwert von unter
15ng/dl erreicht. Die aktuelle Leitlinie der European Association of Urology (EAU) empfiehlt
daher als Zielwert der chemischen Kastration Testosteronspiegel von unter 20ng/dl. Dieser Zielwert
wird untermauert durch eine aktuelle Untersuchung von Klotz und Kollegen [2]. Diese konnte nachweisen,
dass die Senkung des Testosteronspiegels auf unter 20ng/dl (0,7nmol/l) im ersten Jahr der Therapie
mit einem signifikant verlängerten Überleben (cause specific survival, CSS) sowie anhaltender
Sensitivität auf die ADT korreliert (Abb.).
Testosteronspiegel unter 20ng/dl im ersten Jahr der Therapie entscheidend
In die Auswertung wurden insgesamt 626 PCa-Patienten aus der PR-7-Studie [3] einbezogen, die mit
einem LHRH (luteinisierendes Hormon-Releasing-Hormon)-Agonisten behandelt wurden. Die Analyse von
Klotz et al. zeigt nun, dass Patienten, die im ersten Jahr der Therapie den Zielwert von unter 20 ng/dl
erreichten, ein um 29 Prozent geringeres Risiko für die Progression zur Kastrationsresistenz hatten.
Zudem war bei diesen Patienten das Risiko, an ihrer Erkrankung zu versterben, signifikant niedriger (p=0,024).
Bis zu 37,5 Prozent der Patienten, die mit LHRH (luteinisierendes Hormon Releasing-Hormon)-Agonisten
behandelt werden, erreichen den Zielwert von unter 20 ng/dl nicht, so die Autoren. Sie empfehlen eine
regelmäßige Messung des Testosteronwertes, insbesondere im ersten Jahr, jeweils vor der nächsten
Injektion der ADT sowie bei unzureichendem Ansprechen einen Wechsel des Präparates in Erwägung zu ziehen.
Eligard® mit dem Wirkstoff Leuprorelinacetat ist für die Behandlung des hormonabhängigen,
fortgeschrittenen Prostatakarzinoms und in Kombination mit Radiotherapie für die Behandlung von
lokalisiertem Hochrisiko- und lokal fortgeschrittenem hormonabhängigem Prostatakarzinom indiziert.
Es wird als Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in der so genannten
Atrigel®-Depottechnologie angeboten. Diese wird je nach Dosierung (7,5mg, 22,5mg oder 45mg)
einmal im Monat oder alle drei bzw. sechs Monate subkutan verabreicht und bildet ein Arzneimitteldepot,
das über den jeweiligen Zeitraum kontinuierlich Leuprorelinacetat freisetzt. Die Zulassungsstudien
mit Eligard® haben gezeigt, dass es bei ca. 90 Prozent der Patienten den Testosteronspiegel
verlässlich auf Werte unter 20ng/dl senkt [4,5,6]. Testosterondurchbrüche sind mit weniger als
einem Prozent sehr selten. Auch der PSA (Prostataspezifisches Antigen)-Wert konnte in den Studien
signifikant gesenkt werden. Die Behandlung war darüber hinaus gut verträglich. Die am häufigsten
berichteten Nebenwirkungen waren milde bis moderate Hitzewallungen. In der praktischen Anwendung
haben sich Wirksamkeit und Verträglichkeit von Eligard® ebenfalls umfassend bestätigt.
In verschiedenen klinischen Studien konnte Eligard® (Leuprorelinacetat) zeigen, dass es bei der
großen Mehrzahl der Patienten den Testosteronspiegel verlässlich auf Werte unter 20ng/dl (0,7nmol/l) senkt.
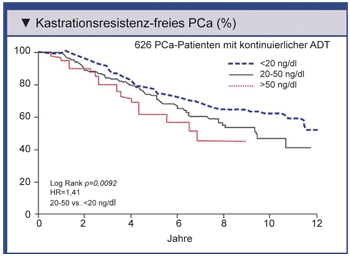
Abb.: Klotz et al. konnten zeigen, dass bei Patienten, deren
Testosteronspiegel unter 20 ng/dl lag, die Progression zur Entwicklung einer Kastrationsresistenz
hinausgezögert wird [2].
Eligard® senkt beim Großteil der Patienten den Testosteronspiegel unter 20ng/dl
Autor: Monika Funck, Köln
Literatur:
[1] Mottet N, et al. 2016. EAU Guidelines on Prostate Cancer update 2016, online publiziert unter: uroweb.org
[2] Klotz L, et al. 2015. J Clin Oncol 33:1151-1156
[3] Crook JM, et al. 2012. N Engl J Med 367:895-903
[4] Perez-Marreno R, et al. 2002. Clinical Therapeutics 2002;24:1902-1914
[5] Chu FM, et al. 2002. The Journal of Urology 168:1199-1203
[6] Crawford ED, et al. 2006. The Journal of Urology 175:533-536.
Mit freundlicher Unterstützung Astellas Pharma GmbH, München.
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz