Neue Hoffnung für Patienten mit Knochenmetastasen
Mit XGEVA® (Denosumab 120 mg q4w) steht seit kurzem ein Medikament zur Verfügung, das bei
erwachsenen Patienten mit soliden, bereits in die Knochen metastasierten Tumoren neue Maßstäbe in der Prävention
skelettbezogener Komplikationen (SRE) setzt. Die Vorteile der neuen Substanz mit innovativem Wirkmechanismus
erläuterten renommierte Experten anlässlich einer Pressekonferenz des Unternehmens Amgen in München.
Die Marktzulassung von Denosumab beruht auf drei Head-to-Head Studien der Phase 3 mit insgesamt mehr als 5.700 Patienten,
in denen die Wirksamkeit von Denosumab hinsichtlich der Verzögerung von SRE gegenüber der bestehenden Standardtherapie
mit Zoledronsäure untersucht wurde.
Eine integrierte Analyse aus den drei Zulassungsstudien belegt die Überlegenheit des neuen Wirkstoffs bei mehr als
50 soliden Tumorentitäten [1]. Im Vergleich zu Zoledronsäure konnte Denosumab das Auftreten skelettbezogener
Ereignisse bei Patienten mit fortgeschrittenen soliden Tumoren und Knochenmetastasen um median 8,2 Monate verzögern,
erläuterte Prof. Dr. Ingo Diel (Mannheim). Bei Patienten, die in den Studien mit Denosumab behandelt wurden, traten SRE
später und seltener auf. Das Risiko eines ersten oder nachfolgenden SRE war unter dem neuen Wirkstoff im Vergleich zu
Zoledronsäure um 18% verringert, betonte Diel. Die Wirkung von Denosumab zeigte sich in den Studien konsistent über
alle SRE-Typen und solide Tumoren hinweg [1].
Skelettbezogene Ereignisse sind für die Patienten meist mit erheblichen Schmerzen verbunden. Auch in dieser Hinsicht
bringt eine Denosumab-
Für den behandelnden Arzt und die Patienten hat Denosumab noch weitere Vorteile: Akute-
Insgesamt war die Anzahl unerwünschter sowie schwerwiegender unerwünschter Ereignisse in beiden Behandlungsgruppen vergleichbar.
Die Rate an Kieferosteonekrosen (ONJ) unterschied sich nicht signifikant unter den beiden Substanzen. ONJ traten insgesamt in
niedriger Inzidenz (1-2% der Patienten) und mit keinem statistisch signifikanten Unterschied zwischen den beiden Studienarmen
auf. Unter Denosumab wurde häufiger eine Hypokalzämie beobachtet, die aber generell nicht symptomatisch oder mit klinischen
Folgen verbunden war. Gesamt-überleben und progressionsfreies Überleben waren in den Behandlungsgruppen in allen drei Studien
vergleichbar.
Ergebnisse von weiteren noch laufenden Studien lassen erahnen, dass das Potential von Denosumab 120 mg im onkologischen
Bereich noch lange nicht ausgeschöpft ist. So zeigt die Phase-3-Studie 147, dass das knochenmetastasenfreie Überleben bei Männern
mit kastrationsresistentem Prostatakarzinom, das sich noch nicht auf den Knochen ausgebreitet hat, um 4,2 Monate verlängert werden
konnte [3, 4]. Eine Phase 3-Studie, bei der es um eine adjuvante Behandlung von Frauen mit frühem
Hochrisiko-
Wir gehen davon aus, dass dieser Wirkstoff noch einiges an Potenzial bietet, fassten Diel und Overkamp in einem gemeinsamen
Ausblick zusammen. Zusätzliche Studien werden die weiteren Möglichkeiten von Denosumab im onkologischen Bereich aufzeigen,
so die Experten.
Referenzen:
Mehr Lebensqualität für Patienten zusätzliche 8,2 Monate ohne SRE
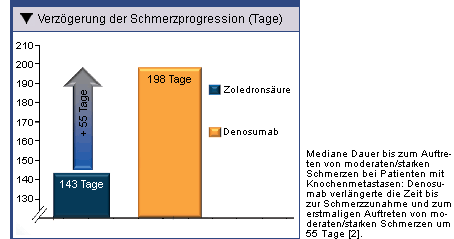
Verzögerte Schmerzprogression
Gute Verträglichkeit und einfache Anwendung
Positive Studienergebnisse zur Prävention von Knochenmetasen
Malgorzata Klafke
Quelle: Pressekonferenz XGEVA®: Neue Hoffnung für Patienten mit Knochenmetastasen am 09.09.2011 in München.
Veranstalter: Amgen GmbH.
[1] Lipton A et al, abstract 1249P, ESMO 2010
[2] Cleeland CS, et al. Ann Oncol 2010;21:8s (Abstract 1248P)
[3] Amgen® Press Release 13. Dezember 2010: www.amgen.com/media
[4] Präsentation Smith MR, et al. Denosumab to Prolong Bone Metastasis-Free Survival in Men With Castrate-Resistant
Prostate Cancer: Results of a Global Phase 3, Randomized, Double-Blind Trial. AUA 2011, Washington.
Druckversion (pdf)
Denosumab setzt neue Maßstäbe hinsichtlich der Prävention skelettbezo-
© 2003-2024 pro-anima medizin medien
–
impressum
–
mediadaten
–
konzeption
–
datenschutz